
Porte COUPE FEU à 1 vantail
د.ت 1.240,000 HT

Douche lave yeux de sécurité 1100
د.ت 2.860,000 HT
Demi masque DONALD FFP2 NR D
د.ت 1,600 HT
- Le demi-masque DONALD FFP2 NR D est un produit médical non stérile ŕ usage unique, de type II R.
- Il est conforme aux exigences de la en 14683:2019 avec une durée d’utilisation limitée, jusqu’a un maximum de 8 heures.
- Il a une efficacité de filtration bactérienne (BFE) de ≥ 98,0 %.
- L’utilisation du respirateur est approuvée dans des environnements médicaux oů il y a un risque d’éclaboussure de liquides corporels.
Rupture de stock
0
personne regarde ce produit maintenant !
UGS :
DONALD FFP2 NR D
Catégorie : Masques anti-particules
Description
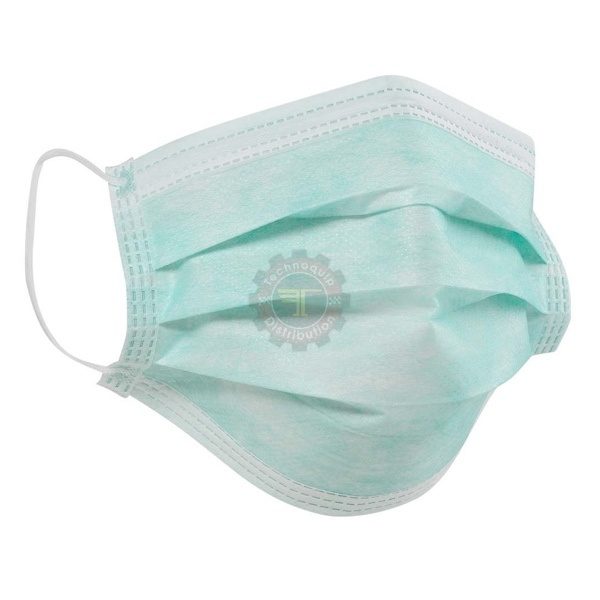
Demi masque DONALD FFP2 NR D
Objet de Demi masque DONALD FFP2 NR D :
- Demi masque DONALD FFP2 NR D est destiné ŕ la protection dans les endroits exposés ŕ des matičres infectieuses et infectieuses oů il y a un risque d’éclaboussure de liquides corporels.
- Il est utilisé pour couvrir la bouche, le nez et le menton. .
- Le produit constitue une barrière limitant la transmission d’un agent infectieux et protégeant les voies respiratoires.
- Il empêche la propagation des micro-organismes en suspension dans l’air, réduisant ainsi le risque d’infection par le personnel médical.
- Son utilisation garantit des conditions de traitement stériles et protège le patient contre les virus / bactéries, par exemple lors des procédures médicales.
- Le Demi masque DONALD FFP2 NR D est également destiné être utilisé par le personnel médical et les patients en cas d’exposition au sang et d’autres liquides corporels potentiellement infectieux.
- Il es t également conçu pour protéger le système respiratoire contre les aérosols de particules solides, les aérosols à base d’eau (poussière, fumée) et les aérosols phase dispersée liquide (brouillard).
- pour lesquels la VLE est ≤0,05 mg/m3 tant que la concentration en phase dispersée ne dépasse pas 10 x VLE. (Valeur limite)
Exigences de Demi masque DONALD FFP2 NR D:
- Les demi-masques de classe DONALD FFP2 NR D sont conformes au règlement (UE) 2017/745 du Parlement européen et du Conseil du 5 avril 2017 relatif aux produits médicaux, modifiant la directive 2001/83/CE, le règlement (CE) n° 178/2002 et le règlement (CE) n° 1223/2009 et abrogeant les directives 90/385/CEE et 93/42/CEE du Conseil (Texte présentant de l’intérêt pour l’EEE).
- Les demi-masques DONALD FFP2 NR D demi-masques respiratoires ont été conçus et mis sur le marché conformément au règlement du Parlement européen et du Conseil (UE) 2016/425 du 9 mars 2016 relatif aux équipements de protection individuelle et abrogeant la directive 89/686/CEE du Conseil.
- EN 14683:2019 + AC:2019 Masques faciaux médicaux – exigences etméthodes d’essai
- EN ISO 15223-1:2021 Dispositifs médicaux — Symboles ŕ utiliser avec les informations ŕ fournir par le fabricant — Partie 1: Exigences générales
- EN ISO 20417:2021 Dispositifs médicaux — Informations ŕ fournir par le fabricant
- EN ISO 14971:2019 Dispositifs médicaux — Application de la gestion des risques aux dispositifs médicaux
- Norme nationale PN-EN 149:2001 + A1:2010, transposant les normes harmonisées européennes EN 149:2001 + A1:2009,
- Le National Standard PN-E-05204:1994 p.3.2.2 f relatif aux espaces de risque d’explosion, qui est confirmé par un avis positif de l’Institut de l’industrie biologique de Varsovie,
- Exigences relatives à l’innocuité pour la santé de l’utilisateur des matériaux utilisés, ce qui est confirmé par un avis positif de l’Institut de médecine du travail de Lodz.
Articles similaires
Informations complémentaires
| Marque |
|---|
Avis (0)
Note 0 sur 5
0 reviews
Note 5 sur 5
0
Note 4 sur 5
0
Note 3 sur 5
0
Note 2 sur 5
0
Note 1 sur 5
0
Seuls les clients connectés ayant acheté ce produit ont la possibilité de laisser un avis.
Produits similaires
Masque anti poussière FFP2 ou FFP3 3M
Note 0 sur 5
En rupture
د.ت 10,000 – د.ت 15,800 HT
Choix des options
Ce produit a plusieurs variations. Les options peuvent être choisies sur la page du produit
Masque anti-poussière à filtre en plastique
Note 0 sur 5
En stock
د.ت 1,550 HT
Choix des options
Ce produit a plusieurs variations. Les options peuvent être choisies sur la page du produit












































































































































































































































































































































Avis
Effacer tous les filtresIl n’y a pas encore d’avis.